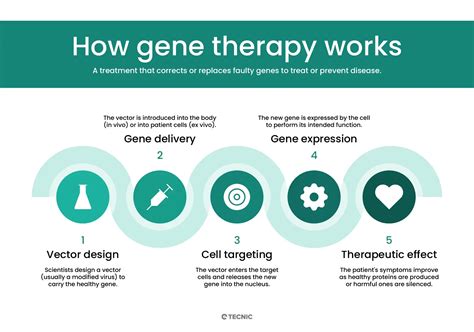
De CRISPR-Cas-technologie heeft de wetenschap op zijn kop gezet met zijn ongekende precisie in het modificeren van DNA. Deze revolutionaire methode opent deuren naar talloze mogelijkheden, van het bestrijden van erfelijke ziekten en malaria tot het creëren van nieuwe diersoorten en het aanpassen van gewassen. De potentiële impact is enorm, en de discussie over de ethische implicaties is dan ook in volle gang.
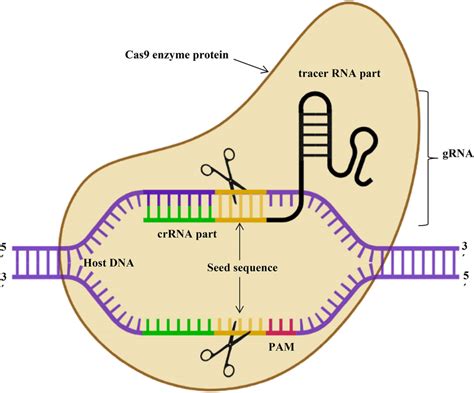
Wat is CRISPR-Cas en hoe werkt het?
CRISPR staat voor 'clustered regularly interspaced palindromic repeats'. Dit is een natuurlijke afweermechanisme dat bacteriën al miljarden jaren gebruiken om virussen uit te schakelen. Wetenschappers hebben dit mechanisme ontdekt en aangepast om het te gebruiken als een moleculair schaartje dat heel gericht kan knippen in het DNA van elke cel. Het proces kan worden vergeleken met het verspreiden van foto's van criminelen door de politie; wanneer een bacterie een stukje viraal DNA herkent dat overeenkomt met een opgeslagen 'foto', stuurt het een moleculair schaartje (het Cas-eiwit, waarvan Cas9 de bekendste is) om het DNA van het virus kapot te knippen.
Wetenschappers kunnen nu zelf bepalen welk stukje DNA er geknipt wordt door het schaartje de juiste 'foto' mee te geven, oftewel een klein stukje genetische code. Dit maakt het mogelijk om zeer nauwkeurig veranderingen aan te brengen in het DNA, tot op gen-niveau. Na het knippen van een ongewenst gen, kan de breuk gerepareerd worden met een stukje DNA waarin de fout is hersteld. Deze methode maakt het mogelijk om zeer precies en efficiënt in het DNA te knippen en plakken.
De ontdekking van deze techniek leverde Jennifer Doudna en Emmanuelle Charpentier in 2020 de Nobelprijs voor Scheikunde op. De techniek wordt voortdurend verder ontwikkeld, met methoden zoals 'prime editing' die het mogelijk maken om niet alleen een heel gen te knippen, maar ook de bouwstenen van een enkel gen zeer nauwkeurig aan te passen, wat kan leiden tot minder bijwerkingen.
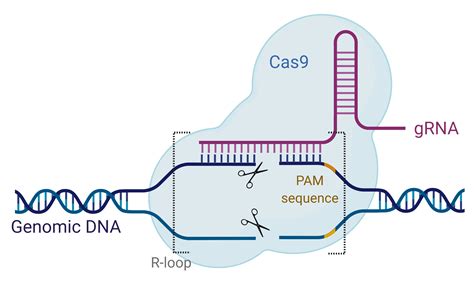
Toepassingen van CRISPR-Cas
Medische doorbraken
De medische mogelijkheden van CRISPR-Cas zijn enorm. Tien patiënten, waaronder twee Nederlanders, zijn dankzij een nieuwe gentherapie met CRISPR-Cas bijna volledig hersteld van de klachten van hun erfelijke zwellingsziekte. Deze techniek maakt het mogelijk om aanpassingen te doen aan genen die ziekten veroorzaken. Voortplantingsbioloog Sjoerd Repping verwacht dat erfelijke ziekten binnen korte tijd zelfs uit menselijke embryo's verwijderd kunnen worden. Hoewel er nog steeds risico's bestaan, zoals het per ongeluk beschadigen van andere genen, boekt de wetenschap hierin grote vooruitgang.
Naast het repareren van genen, biedt CRISPR-Cas ook de mogelijkheid om genen te vervangen door 'betere' genen. Dit opent de weg naar het aanpassen van embryo's naar onze eigen wens, de zogenaamde 'designer baby's'. Eigenschappen als sterkere botten, betere spiergroei of een specifieke oogkleur zouden in theorie mogelijk zijn, mits een enkel gen voor die eigenschap verantwoordelijk is. Complexere eigenschappen zoals intelligentie, waarbij vele genen een rol spelen, zijn nog niet te manipuleren.
CRISPR-Cas9-technologie voor genoomeditie
Agrarische innovaties
In de landbouw wordt CRISPR-Cas ingezet voor het veredelen van planten en zaden. Met deze revolutionaire gentechniek kunnen gewassen heel gericht worden verbeterd, bijvoorbeeld voor een hogere opbrengst of een lagere waterbehoefte. Veredeling van planten is al eeuwenlang de manier om voedselgewassen te kweken die beter bestand zijn tegen ziekten en klimaatverandering. Gerichte mutatietechnieken in het laboratorium, zoals CRISPR-Cas, bieden hierbij snellere en betere resultaten.
De Europese Commissie heeft de regels voor de toepassing van CRISPR-Cas in gewassen versoepeld, waardoor het telen van genetisch gemodificeerde gewassen in landen als Argentinië al langer is toegestaan. In Nederland staan Nederlanders niet onwelwillend tegenover de techniek, en brancheorganisaties zien potentieel voor snellere plantenveredeling en het weerbaarder maken van planten tegen schimmels en virusziektes.

Andere mogelijke toepassingen
De mogelijkheden van CRISPR-Cas reiken verder dan geneeskunde en landbouw. Wetenschappers onderzoeken het potentieel om bacteriën te creëren die olie of plastic kunnen opeten, varkens te kweken waarin menselijke organen kunnen groeien, of zelfs uitgestorven dieren weer tot leven te wekken. Onderzoekers richten zich onder leiding van geneticus George Church op het tot leven wekken van de mammoet, niet om perfecte kopieën te maken, maar om olifanten de karakteristieken van mammoeten te geven, zodat zij in staat zijn te overleven in het ijzige klimaat van de toendra's. Dit zou kunnen bijdragen aan het vertragen van het smelten van het Arctisch gebied.
Het is belangrijk op te merken dat het terugbrengen van uitgestorven diersoorten complexe vereisten kent: er moet voldoende DNA over zijn, er moet een nauw verwante soort zijn om het DNA in te brengen, en de soort mag niet langer dan 800.000 jaar geleden zijn uitgestorven. Dinosauriërs tot leven wekken behoort hierdoor niet tot de mogelijkheden.
Ethische dilemma's en bezwaren
Naast de vele mogelijkheden roept CRISPR-Cas ook belangrijke ethische vragen op. De vraag naar de wenselijkheid van 'designer baby's' is een van de meest prangende kwesties. Tegenstanders van DNA-manipulatie uiten zorgen over het 'voor God spelen' en de onvoorspelbare gevolgen van het aanpassen van genen. Er bestaat onzekerheid over mogelijke ongewenste bijeffecten, zoals afweerreacties bij mensen.
Hoewel er in sommige landen, zoals Engeland, al wetgeving is die het bewerken van embryo's voor wetenschappelijk onderzoek toestaat, is het in veel landen nog niet toegestaan om deze bewerkte embryo's tot baby's te laten uitgroeien. Toch is er een trend naar wetsverruiming, ook in Nederland, waar de Gezondheidsraad zich inzet voor het legaliseren van genetisch bewerken van embryo's. Vergelijkingen worden gemaakt met de acceptatie van IVF-technologie, die destijds ook op veel kritiek stuitte.
CRISPR-Cas9-technologie voor genoomeditie
Gene Drives: CRISPR in het Kwadraat
Een verdere ontwikkeling van CRISPR-Cas zijn de zogenaamde 'gene drives'. Deze methode maakt het mogelijk om niet alleen aan individuen, maar aan gehele populaties te sleutelen. Door een precieze mutatie aan te brengen in de geslachtscellen van een organisme, kan deze mutatie met een veel grotere kans worden doorgegeven aan nakomelingen, waardoor een eigenschap zich snel en blijvend door een hele populatie kan verspreiden.
Wetenschappers hebben succesvol een gene drive ingebouwd in muggen, waardoor deze ongevoelig werden voor de malariaparasiet. Dit resulteerde in een populatie malariamuggen die onschadelijk is voor de mens. Hoewel het uitroeien van ziekten als malaria een droomscenario is, brengt gene drive ook risico's met zich mee. Eenmaal verspreid, is een verandering moeilijk terug te draaien en zijn de langetermijngevolgen onduidelijk. Er bestaat bezorgdheid dat het uitroeien van een ziekte kan leiden tot de opkomst van een nog gevaarlijkere parasiet, met consequenties voor het ecosysteem.